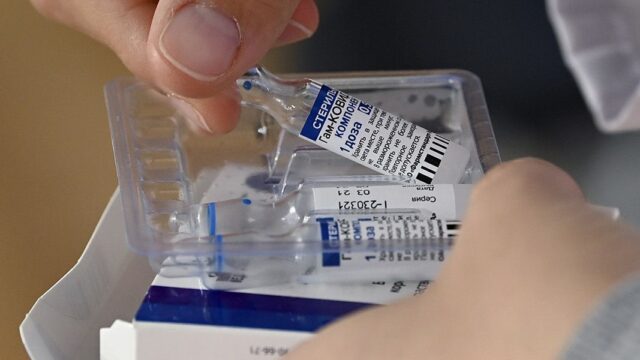
Разработчики российской вакцины от коронавируса «Спутник V» не предоставили европейскому регулятору ряд данных, которые являются стандартными требованиями для одобрения препаратов в Евросоюзе. Об этом 13 июля сообщает Reuters со ссылкой на информированные источники.
10 июня истек крайний срок предоставления Европейскому агентству по лекарственным средствам полных данных о клинических испытаниях вакцины. Также не были получены данные о процессе ее производства. В связи с этим в июне рассмотрение эффективности и безопасности российского препарата было отложено.
Кроме того, французские ученые, которые проводили оценку «Спутника V» перед началом его рассмотрения регулятором, выяснили, что разработчики вакцины не смогли подтвердить, что его базовый компонент соответствует одному из регламентов Евросоюза.
Среди данных о клинических испытаниях вакцины также отсутствовала информация о побочных эффектах и их последствиях. Из предоставленной регулятору информации также непонятно, как разработчики «Спутника V» отслеживали результаты участников испытаний, получивших плацебо.
Европейский регулятор начал оценку российской вакцины в марте, и его решение ожидалось в мае или июне. Из-за задержек, даже при оперативном предоставлении недостающих данных, изучение препарата вряд ли завершится до конца лета, утверждает один из источников Reuters.
Собеседники агентства полагают, что возникшие проблемы связаны с недостатком у разработчиков «Спутника V» из центра Гамалеи опыта работы с зарубежными регуляторами.
В Российском фонде прямых инвестиций (РФПИ), который занимается продвижением российской вакцины на зарубежных рынках, назвали информацию источников Reuters частью кампании по дезинформации против «Спутника V», которую организовало «западное фармацевтическое лобби».
В РФПИ напомнили, что препарат одобрили в десятках стран и нигде не было зафиксировано серьезных побочных эффектов. По поводу претензий французских ученых в фонде заявили, что его базовый клеточный компонент полностью соответствует требованиям европейского регулятора.
Один из источников Reuters сказал, что у иностранных регуляторов нет причин сомневаться в эффективности и надежности «Спутника V», и главные проблемы у его разработчиков связаны с неполнотой данных, недостаточной документацией по методологии испытаний и несоблюдением стандартных требований, предъявляемых к лекарствам в разных странах.